P 메드팩토, 선택과 집중 전략으로 전환...조기 상업화 '승부수'
등록 2022-08-17 오전 8:30:29
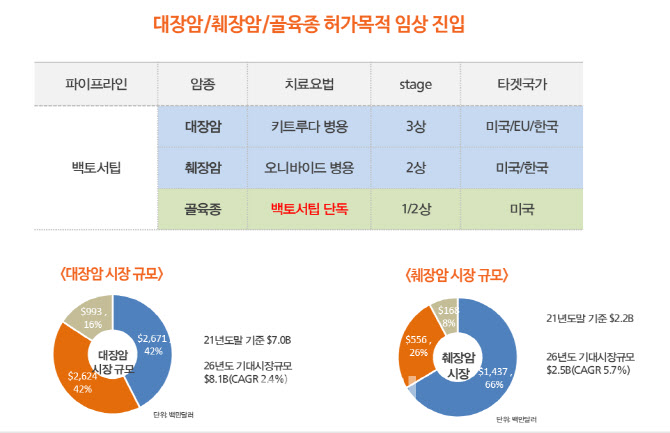
- 백토서팁 임상, 대장암·췌장암·골육종 3개 적응증에 집중
대장암, 머크 전폭 지원 등에 업고 3상 연내 진입
골육종·췌장암, 희귀의약품 지정...2상 중 상업화 시도
"2025년까지 대장암·췌장암 상용화 목표"
팜이데일리 프리미엄 기사를 무단 전재·유포하는 행위는 불법이며 형사 처벌 대상입니다.
이에 대해 팜이데일리는 무관용 원칙을 적용해 강력히 대응합니다.
이에 대해 팜이데일리는 무관용 원칙을 적용해 강력히 대응합니다.
이 기사는 2022년8월17일 8시30분에 팜이데일리 프리미엄 콘텐츠로 선공개 되었습니다.
구독하기
[이데일리 김지완 기자] 메드팩토(235980)가 선택과 집중 전략으로 백토서팁 조기 상용화에 나선다.
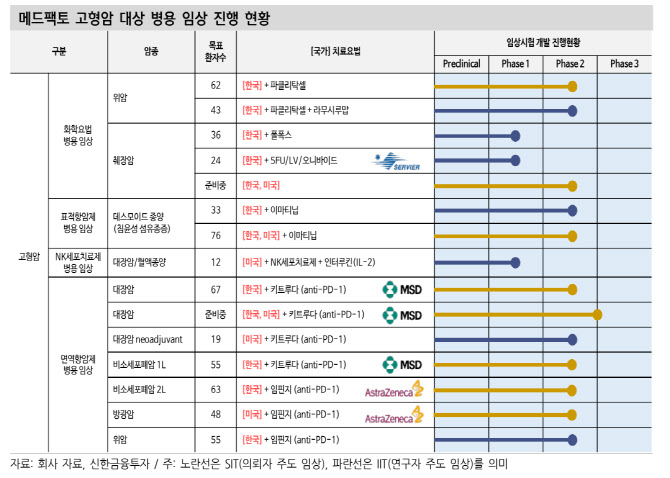
16일 메드팩토에 따르면, 메드팩토는 앞으로 백토서팁에 대해 골육종, 췌장암, 대장암 등 3개 적응증에 임상을 집중할 계획이다.
암은 ‘TGB-베타1’을 생성해 주변 섬유세포에 작용한다. 이 과정에서 섬유질은 암을 둘러싸 항암제 침투를 막아서는 벽이 된다. 백토서팁은 이 방어벽을 뚫고 약물을 암세포 속으로 들어가게 해주는 역할을 한다. 백토서팁이 모든 암종에서 효과를 발현할 수 있는 이유다. 이런 이유로 메드팩토는 백토서팁을 골육종, 위암, 췌장암, 데스모이드 종양(침윤성 섬유종증), 대장암, 혈액종양, 비소세포폐암, 방광암, 위암 등 다양한 적응증에 임상을 진행해왔다.
“허가용 임상에 집중...조기 상용화 목표”
메드팩토는 향후 백토서팁 허가용 임상에 집중할 계획이다. 메드팩토 관계자는 “작년까지 다양한 암종에서 백토서팁 임상을 진행했고, 효과를 확인했다”면서 “올 상반기 백토서팁을 골육종, 췌장암, 대장암 등의 적응증에 조기 상용화하는 방향으로 목표를 수정했다”고 밝혔다. 이어 “역량이 분산이 약품 상용화에 걸림돌이 된다고 판단했기 때문”이라고 덧붙였다.
실제로 메드팩토는 지난 5월 33명의 환자를 대상으로 진행 중이던 데스모이드 종양 국내 임상 2상을 자진철회했다. 메드팩토 관계자는 “데이터는 좋았지만 희귀병에 시장성 낮은 적응증까지 임상을 수행하긴 어려웠다”고 이유를 밝혔다.
대장암, 머크 전폭 지원 등에 업고 올해 3상 진입
메드팩토가 밝힌 3개 적응증 가운데 가장 진도가 빠른 것은 대장암이다. 머크의 ‘키트루다’와 병용투여로 진행되는 대장암 임상은 글로벌 임상 3상을 목전에 두고 있다.
메도팩토 관계자는 “키트루다+백토서팁 임상 3상은 빠르면 연말, 늦어도 내년 초 미국 식품의약국(FDA)에 ‘임상계획승인’(IND)을 신청할 것으로 예상된다”고 밝혔다. ‘키트루다+백토서팁’의 임상 2상 결과는 아직 발표하지 않았지만, 임상 3상을 준비 중인 것으로 미루어 성공적인 결과가 나온 것으로 추측된다.
키트루다+백토서팁 임상 3상은 200~300명을 대상으로 미국, 한국, 유럽 40여 개 사이트에서 진행될 예정이다. 업계에선 키트루다+백토서팁 임상 3상 중간데이터 결과가 잘 나오면, 치료제 품목허가 조기승인 신청을 할 것으로 내다봤다.
클리닉트라이얼과 머크에 따르면 현재 키트루다 관련 임상 수는 약 1500여 개에 이른다. 이중 임상 2b상~3상 단계에 있는 후보물질은 148개다. 전체 키트루다 관련 임상에서 머크로부터 키트루다를 무상 제공받는 임상은 총 13건이다. 백토서팁은 13개 약물 중 하나다.
키트루다 약가가 1인당 1억원을 호가한다는 점에서 머크의 키트루다+백토서팁 임상 3상 지원액만 최소 200억원에서 최대 300억원에 이른다는 계산이다.
FDA 희귀의약품 지정으로 상용화 가능성 높아
췌장암 치료제도 FDA 연내 임상 2상 진입을 예고했다. 메드팩토는 현재 ‘백토서팁+오니바이드’와 ‘백토서팁+폴폭스’ 등 2종류의 췌장암 임상을 각각 진행 중이다. 메드팩토는오는 9월 백토서팁+오니바이드 병용요법에 대해 FDA 임상 2상 IND를 신청할 계획이다.
메드팩토 관계자는 “백토서팁+오니바이드 임상 1b상은 결과발표만 안 했을 뿐, 안전성과 유효성이 모두 확인됐다”면서 “오니바이드 병용요법 임상 2상 허가용 임상”이라고 말했다.
그는 “백토서팁+오니바이드 병용요법은 지난해 FDA로부터 ‘희귀의약품’(ODD)로 지정돼 조기 상용화가 유리하다”면서 “2상 중간데이터가 잘 나오면 임상 중에라도 품목허가 신청을 할 계획”이라고 부연했다.
단독요법으로 진행되는 골육종 치료제 상용화 작업도 이미 닻을 올렸다. 메드팩토는 지난달 FDA에 골육종 임상 1/2상 IND를 제출했다. 골육종은 뼈 또는 연골에서 발생하는 악성종양을 말한다.
골육종은 환자 중 20~25%는 암이 폐로 전이돼 항암치료 중 사망하는 사례가 부지기수다. 골육종은 전체 육종암 가운데 6%를 차지한다. 이 치료제 역시 지난해 FDA로부터 희귀의약품으로 지정됐다.
메드팩토 측은 “백토서팁은 골육종에 대해서도 희귀의약품으로 지정받아 조기 상업화 가능성이 높다고 판단하고 있다”고 말했다. 그는 이어 “현재는 기술수출보단 끝까지 임상을 진행해 상용화까지 하기로 했다”면서 “오는 2025년까지 대장암·췌장암에 대해선 상용화를 하는 것이 목표”라고 밝혔다.
|
16일 메드팩토에 따르면, 메드팩토는 앞으로 백토서팁에 대해 골육종, 췌장암, 대장암 등 3개 적응증에 임상을 집중할 계획이다.
암은 ‘TGB-베타1’을 생성해 주변 섬유세포에 작용한다. 이 과정에서 섬유질은 암을 둘러싸 항암제 침투를 막아서는 벽이 된다. 백토서팁은 이 방어벽을 뚫고 약물을 암세포 속으로 들어가게 해주는 역할을 한다. 백토서팁이 모든 암종에서 효과를 발현할 수 있는 이유다. 이런 이유로 메드팩토는 백토서팁을 골육종, 위암, 췌장암, 데스모이드 종양(침윤성 섬유종증), 대장암, 혈액종양, 비소세포폐암, 방광암, 위암 등 다양한 적응증에 임상을 진행해왔다.
“허가용 임상에 집중...조기 상용화 목표”
메드팩토는 향후 백토서팁 허가용 임상에 집중할 계획이다. 메드팩토 관계자는 “작년까지 다양한 암종에서 백토서팁 임상을 진행했고, 효과를 확인했다”면서 “올 상반기 백토서팁을 골육종, 췌장암, 대장암 등의 적응증에 조기 상용화하는 방향으로 목표를 수정했다”고 밝혔다. 이어 “역량이 분산이 약품 상용화에 걸림돌이 된다고 판단했기 때문”이라고 덧붙였다.
실제로 메드팩토는 지난 5월 33명의 환자를 대상으로 진행 중이던 데스모이드 종양 국내 임상 2상을 자진철회했다. 메드팩토 관계자는 “데이터는 좋았지만 희귀병에 시장성 낮은 적응증까지 임상을 수행하긴 어려웠다”고 이유를 밝혔다.
|
대장암, 머크 전폭 지원 등에 업고 올해 3상 진입
메드팩토가 밝힌 3개 적응증 가운데 가장 진도가 빠른 것은 대장암이다. 머크의 ‘키트루다’와 병용투여로 진행되는 대장암 임상은 글로벌 임상 3상을 목전에 두고 있다.
메도팩토 관계자는 “키트루다+백토서팁 임상 3상은 빠르면 연말, 늦어도 내년 초 미국 식품의약국(FDA)에 ‘임상계획승인’(IND)을 신청할 것으로 예상된다”고 밝혔다. ‘키트루다+백토서팁’의 임상 2상 결과는 아직 발표하지 않았지만, 임상 3상을 준비 중인 것으로 미루어 성공적인 결과가 나온 것으로 추측된다.
키트루다+백토서팁 임상 3상은 200~300명을 대상으로 미국, 한국, 유럽 40여 개 사이트에서 진행될 예정이다. 업계에선 키트루다+백토서팁 임상 3상 중간데이터 결과가 잘 나오면, 치료제 품목허가 조기승인 신청을 할 것으로 내다봤다.
클리닉트라이얼과 머크에 따르면 현재 키트루다 관련 임상 수는 약 1500여 개에 이른다. 이중 임상 2b상~3상 단계에 있는 후보물질은 148개다. 전체 키트루다 관련 임상에서 머크로부터 키트루다를 무상 제공받는 임상은 총 13건이다. 백토서팁은 13개 약물 중 하나다.
키트루다 약가가 1인당 1억원을 호가한다는 점에서 머크의 키트루다+백토서팁 임상 3상 지원액만 최소 200억원에서 최대 300억원에 이른다는 계산이다.
FDA 희귀의약품 지정으로 상용화 가능성 높아
췌장암 치료제도 FDA 연내 임상 2상 진입을 예고했다. 메드팩토는 현재 ‘백토서팁+오니바이드’와 ‘백토서팁+폴폭스’ 등 2종류의 췌장암 임상을 각각 진행 중이다. 메드팩토는오는 9월 백토서팁+오니바이드 병용요법에 대해 FDA 임상 2상 IND를 신청할 계획이다.
메드팩토 관계자는 “백토서팁+오니바이드 임상 1b상은 결과발표만 안 했을 뿐, 안전성과 유효성이 모두 확인됐다”면서 “오니바이드 병용요법 임상 2상 허가용 임상”이라고 말했다.
그는 “백토서팁+오니바이드 병용요법은 지난해 FDA로부터 ‘희귀의약품’(ODD)로 지정돼 조기 상용화가 유리하다”면서 “2상 중간데이터가 잘 나오면 임상 중에라도 품목허가 신청을 할 계획”이라고 부연했다.
단독요법으로 진행되는 골육종 치료제 상용화 작업도 이미 닻을 올렸다. 메드팩토는 지난달 FDA에 골육종 임상 1/2상 IND를 제출했다. 골육종은 뼈 또는 연골에서 발생하는 악성종양을 말한다.
골육종은 환자 중 20~25%는 암이 폐로 전이돼 항암치료 중 사망하는 사례가 부지기수다. 골육종은 전체 육종암 가운데 6%를 차지한다. 이 치료제 역시 지난해 FDA로부터 희귀의약품으로 지정됐다.
메드팩토 측은 “백토서팁은 골육종에 대해서도 희귀의약품으로 지정받아 조기 상업화 가능성이 높다고 판단하고 있다”고 말했다. 그는 이어 “현재는 기술수출보단 끝까지 임상을 진행해 상용화까지 하기로 했다”면서 “오는 2025년까지 대장암·췌장암에 대해선 상용화를 하는 것이 목표”라고 밝혔다.
|
김지완 2pac@






![지놈앤컴퍼니, 임상 본격화 기대감에 급등…숨고르기 들어간 바이젠셀[바이오 맥짚기]](https://image.edaily.co.kr/images/vision/files/NP/S/2026/04/PS26043000447b.jpg)
