희귀 염증 질환부터 코로나19까지 커버하는 팔방미인 '악템라'[블록버스터 톺아보기]
[이데일리 김진호 기자]자신이나 가족의 질환 또는 투자 등 목적은 다를 수 있다. 제약바이오에 관심있는 사람이라면 들어봤을 법한 전 세계 블록버스터 약물을 2020년 기준 매출이 높은 순으로 소개한다. 약의 탄생과정부터 그 특징, 비슷한 계열의 경쟁 약물까지 두루 살펴본다.
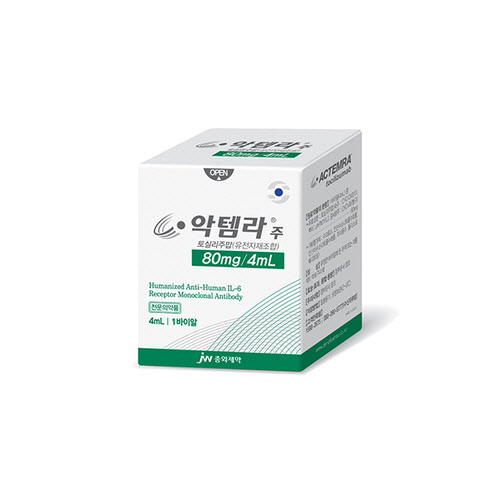
이번에는 스위스 로슈의 염증질환 치료제 ‘악템라’(성분명 토실리주맙)다. 2020년 기준 글로벌 시장 매출액은 약 30억8000만 달러(당시 한화 약 3조6300억원)로 전체 의약품 중 매출 34위를 기록한 블록버스터다.
악템라의 성분인 토실리주맙은 면역 ‘신호전달물질’(사이토카인) 중 하나인 인터류킨(IL)-6의 수용체에 선택적으로 결합하는 단일클론항체다. IL-6은 자가면역질환, 다발성 골수종, 전립선암 등 다양한 질병과 연관된 사이토카인으로 알려졌다.
토실리주맙은 1980년대 일본 오사카대 연구진이 발견했다. 1997년부터 로슈의 자회사인 주가이 파마슈티컬스(쥬가이)가 토실리주맙을 류마티스 관절염 치료제로 개발하기 위한 임상을 시작했다. 쥬가이는 2001년과 2002년 각각 해당 물질을 캐슬만병과 전신성 소아 특발성 관절염 치료제로 개발하려는 추가 임상에도 차레로 착수했다.
류마티스 관절염은 관절의 기능 상실을 일으키는 염증 질환이며, 캐슬만병은 전신의 림프절에서 발생하는 매우 드문 염증 질환이다. 전신성 소아 특발성 관절염 역시 소아의 전신 관절에서 나타나는 염증질환으로 알려졌다. 여러 자가면역질환에 대한 토시리주맙의 효능이 전임상에서 확인되자, 관련 임상을 진행할 수 있었던 셈이다.
2005년 일본 의약당국이 캐슬만병 치료제로 정맥주사형 악템라를 먼저 승인했다. 유럽의약품청(EMA)와 미국 식품의약국(FDA)는 각각 2009년과 2010년에 류마티스 관절염 치료제로 악템라를 승인했다.
이후 FDA와 EMA는 2011년 2세 이상 전신성 소아 특발성 관절염 치료제로 악템라의 적응증을 확대 승인했다. 식품의약품안전처(식약처)도 2012년에 류머티스관절염 치료제로 악템라를 승인했고, 이후 전신성 소아 특발성 관절염, 다과절형 소아 특발성 관절염 적응증을 확대 승인한 바 있다. 현재 각국에서 앞서 말한 악템라의 적응증이 두루 승인돼 환자에게 쓰이고 있는 상황이다.
2010년대 초반 로슈는 악템라의 피하주사(SC)제형 개발에도 성공했다. 국내 도입 사례를 살펴보면 식약처가 2014년 악템라 피하주사제형을 류머티스 관절염 치료제로 승인했다. 식약처는 2020년 거대세포 동맥염 적응증을 해당 약물에 추가했다. 거대세포 동맥염은 심장에서 몸 전체로 혈액을 공급하는 동맥 내벽에서 염증과 괴사가 일어나는 만성 염증 질환으로 ‘측두동맥염’이라고도 불린다. 이와 같은 국내 승인은 해당 적응증으로 이미 유럽과 미국 등에서 악템라 피하주사제형이 승인된 이후 이뤄진 조치였다.
현재 주가이가 악템라의 정맥주사제형과 피하주사제형에 대한 일본 등 일부 아시아 국가 내 판매를 담당하고 있다. 유럽이나 미국 등에서는 로슈와 주가이가 이를 공동으로 판매하고 있다.
특히 해당 약물의 국내 유통은 모두 로슈로부터 판권을 받은 JW중외제약(001060)이 담당하는 중이다. 회사측에 따르면 지난 3월 2세 이상 코로나19 중증환자 대상 치료제로 긴급사용 승인된 정맥주사형 악템라의 매출이 전년 동기 대비 약 56% 증가한 64억원을 기록한 것으로 알려졌다.
한편 지난 7월 셀트리온(068270)이 폴란드 의약품기기등록청(URPL)으로부터 악템라 바이오시밀러 ‘CT-P47’의 임상 3상 계획서를 승인받았다. 셀트리온은 악템라의 피하주사제형과 정맥주사제형 등에 대한 바이오시밀러를 동시에 개발하는 것으로 알려졌다.
이번에는 스위스 로슈의 염증질환 치료제 ‘악템라’(성분명 토실리주맙)다. 2020년 기준 글로벌 시장 매출액은 약 30억8000만 달러(당시 한화 약 3조6300억원)로 전체 의약품 중 매출 34위를 기록한 블록버스터다.
|
악템라의 성분인 토실리주맙은 면역 ‘신호전달물질’(사이토카인) 중 하나인 인터류킨(IL)-6의 수용체에 선택적으로 결합하는 단일클론항체다. IL-6은 자가면역질환, 다발성 골수종, 전립선암 등 다양한 질병과 연관된 사이토카인으로 알려졌다.
토실리주맙은 1980년대 일본 오사카대 연구진이 발견했다. 1997년부터 로슈의 자회사인 주가이 파마슈티컬스(쥬가이)가 토실리주맙을 류마티스 관절염 치료제로 개발하기 위한 임상을 시작했다. 쥬가이는 2001년과 2002년 각각 해당 물질을 캐슬만병과 전신성 소아 특발성 관절염 치료제로 개발하려는 추가 임상에도 차레로 착수했다.
류마티스 관절염은 관절의 기능 상실을 일으키는 염증 질환이며, 캐슬만병은 전신의 림프절에서 발생하는 매우 드문 염증 질환이다. 전신성 소아 특발성 관절염 역시 소아의 전신 관절에서 나타나는 염증질환으로 알려졌다. 여러 자가면역질환에 대한 토시리주맙의 효능이 전임상에서 확인되자, 관련 임상을 진행할 수 있었던 셈이다.
2005년 일본 의약당국이 캐슬만병 치료제로 정맥주사형 악템라를 먼저 승인했다. 유럽의약품청(EMA)와 미국 식품의약국(FDA)는 각각 2009년과 2010년에 류마티스 관절염 치료제로 악템라를 승인했다.
이후 FDA와 EMA는 2011년 2세 이상 전신성 소아 특발성 관절염 치료제로 악템라의 적응증을 확대 승인했다. 식품의약품안전처(식약처)도 2012년에 류머티스관절염 치료제로 악템라를 승인했고, 이후 전신성 소아 특발성 관절염, 다과절형 소아 특발성 관절염 적응증을 확대 승인한 바 있다. 현재 각국에서 앞서 말한 악템라의 적응증이 두루 승인돼 환자에게 쓰이고 있는 상황이다.
2010년대 초반 로슈는 악템라의 피하주사(SC)제형 개발에도 성공했다. 국내 도입 사례를 살펴보면 식약처가 2014년 악템라 피하주사제형을 류머티스 관절염 치료제로 승인했다. 식약처는 2020년 거대세포 동맥염 적응증을 해당 약물에 추가했다. 거대세포 동맥염은 심장에서 몸 전체로 혈액을 공급하는 동맥 내벽에서 염증과 괴사가 일어나는 만성 염증 질환으로 ‘측두동맥염’이라고도 불린다. 이와 같은 국내 승인은 해당 적응증으로 이미 유럽과 미국 등에서 악템라 피하주사제형이 승인된 이후 이뤄진 조치였다.
현재 주가이가 악템라의 정맥주사제형과 피하주사제형에 대한 일본 등 일부 아시아 국가 내 판매를 담당하고 있다. 유럽이나 미국 등에서는 로슈와 주가이가 이를 공동으로 판매하고 있다.
특히 해당 약물의 국내 유통은 모두 로슈로부터 판권을 받은 JW중외제약(001060)이 담당하는 중이다. 회사측에 따르면 지난 3월 2세 이상 코로나19 중증환자 대상 치료제로 긴급사용 승인된 정맥주사형 악템라의 매출이 전년 동기 대비 약 56% 증가한 64억원을 기록한 것으로 알려졌다.
한편 지난 7월 셀트리온(068270)이 폴란드 의약품기기등록청(URPL)으로부터 악템라 바이오시밀러 ‘CT-P47’의 임상 3상 계획서를 승인받았다. 셀트리온은 악템라의 피하주사제형과 정맥주사제형 등에 대한 바이오시밀러를 동시에 개발하는 것으로 알려졌다.
김진호 twok@







![FDA, CAR-T 치료제 접근 장벽 완화[제약·바이오 해외토픽]](https://image.edaily.co.kr/images/vision/files/NP/S/2025/07/PS25071200083b.jpg)
![[르포] 안드로이드 탄생한 보스턴CIC가보니…"K-바이오, 빅딜 마중물"](https://image.edaily.co.kr/images/vision/files/NP/S/2025/07/PS25071401146b.jpg)
![이승호 데일리파트너스 대표 “하반기 바이오 전망 밝다, 다중항체 주목”[바이오 VC 집중조명]①](https://image.edaily.co.kr/images/vision/files/NP/S/2025/07/PS25071500005b.jpg)
